Vörösvérsejtek: a személyre szabott diagnosztika új segítői
Az egy cseppnyi vérünkben jelen lévő néhány ezer fehérvérsejt DNS-éből ma már gyorsan és pontosan meghatározhatjuk a teljes génállományunkat, felderíthetjük a kódoló szakaszokban rejlő öröklődő, ritka génhibákat, de megismerhetjük azt a több millió, a személyünkre vonatkozóan egyedi, kis méretű génváltozatot (ún. polimorfizmust, hiányt vagy ismétlődést) is, amelyeknek szerepük lehet a betegségek kialakulásában, lefolyásában vagy éppen kezelhetőségében.
Míg a fehérjéinket kódoló gének a teljes DNS-állományunknak (a genomunknak) csak néhány százalékát jelentik, a hatalmas tömegű többi DNS-szakasz nem az evolúció „szemete”, hanem szabályozó szereppel rendelkezik, így ezek a génváltozatok éppen a nagy csoportokat érintő, többtényezős betegségek fontos elemei.
A molekuláris genetikai kutatások, a ma már több tízezer ember teljes génállományát és a betegségek egyéni megjelenéseit összekapcsoló (genome-wide association, GWA) vizsgálatok ezen a téren a személyre szabott orvoslás gyors fejlődését ígérik. Kialakult azonban egy rés a génváltozatok feltérképezése, valamint a sejtjeink felépítését és működését valóban érintő elváltozások megismerése között. Emiatt alig ismerjük azokat a genetikai kapcsolatokat, amelyek a fehérjék és lipidek szintjének, működésének szabályozása révén valójában a betegségeket okozzák. Különösen hiányosak az ismereteink a sejtek membránjában elhelyezkedő fehérjék genetikai szabályozásáról, amelyek viszont mind a betegségekben, mind a gyógyszeres kezelésekben kulcsfontosságúak.
Ezen a téren segíthet a vörösvérsejtek vizsgálata, hiszen a kevés fehérvérsejt mellett, ugyanabban az (akár ujjbegyszúrással is könnyen nyerhető) egy csepp vérben több száz millió vörösvérsejt is jelen van. A vörösvérsejtek az oxigén és a szén-dioxid szállítására specializálódott sejtjeink, amelyek a vörös vérfesték fehérjét (a hemoglobint) és az anyagcseréjükhöz szükséges enzimeket a sejtmembrán „zsákjában” tartalmazzák, míg minden más sejtalkotórészt az érésük során eltávolítanak. A sejtmembrán az egyedüli membránjuk, így az 1950–80-as évekig a membránbiológiai kutatások „bölcsőjét” ennek a membránnak a vizsgálata jelentette.
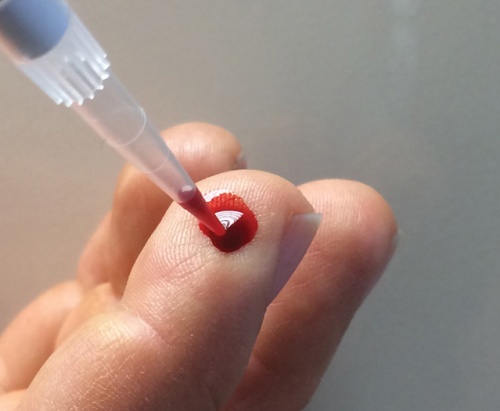 Egy ujjbegyszúrással is könnyen nyerhető egy csepp vérben több száz millió vörösvérsejt is jelen van.
Egy ujjbegyszúrással is könnyen nyerhető egy csepp vérben több száz millió vörösvérsejt is jelen van.Akkoriban azt gondoltuk, hogy ez a membrán csak néhány, a vörösvérsejtre jellemző fehérjét tartalmaz. Ma már tudjuk, hogy ebben a biológiai membránokra általánosan jellemző szerkezetben több százféle (!) membránfehérje található meg, amelyek – elképzelésünk szerint – tükrözik a genetikailag meghatározott emberi membránfehérjék számos jellemzőjét és a kifejeződésük szabályozását is. Ennek magyarázata az lehet, hogy a vörösvérsejtek a vérképző őssejtekből néhány nap alatt alakulnak ki, és igen gyors, aktív kilökési folyamattal szabadulnak meg minden belső sejtszervecskétől. Ugyanakkor, mintegy négy hónapos élettartamuk alatt megőrzik az érés során keletkezett membránfehérjék sokaságát, akár szükség van azokra, akár nincs. Ráadásul, a hosszú élettartam érdekében, az érésükkor megszabadulnak minden fehérjelebontó enzimtől is, így ez a membránfehérje-állomány stabilan és állandóan jelen van. Kutatócsoportunk a membránfehérjék vizsgálatának ezt a feltételezett új aranybányáját próbálja felhasználni a személyre szabott orvosi diagnosztika és kezelések lehetőségeinek kitágítására.
A 2012-ben elindított, és azóta nemzetközi szinten elfogadott szabadalmi beadványunk lényege, hogy a könnyen, nagy számban kinyerhető vörösvérsejtek membránjában célzott antitestek segítségével meghatározzuk az egyes betegségekben fontos fehérjék mennyiségét, majd összehasonlítjuk ezeket az egészséges embereknél, illetve az adott betegségben szenvedőknél mért szintekkel. A megtalált változásokat összekapcsoljuk célzott, az adott fehérjére vonatkozó molekuláris genetikai analízissel. Az elmúlt években sok tekintetben bebizonyosodott elképzelésünk szerint a vörösvérsejt membránfehérjék genetikai vizsgálatokkal kombinálva biomarkerként szolgálhatnak nemcsak diagnosztikai célokra, de a gyógykezelés megtervezéséhez is. Így olyan emberi szövetek (májsejtek, szívizom- vagy idegsejtek) membránfehérjéiről is felvilágosítást kaphatunk, amelyek eredeti környezetükben nem, vagy csak nehezen vizsgálhatók.
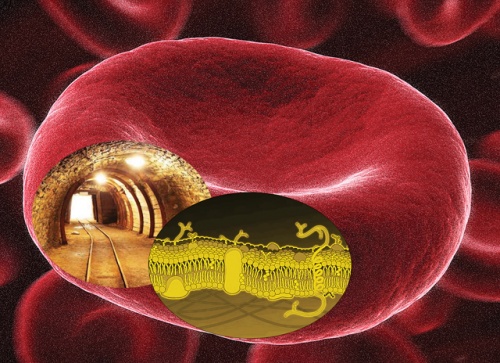 A membránbiológia aranybányája, a vörösvérsejtek membránja.
A membránbiológia aranybányája, a vörösvérsejtek membránja.Természetesen mindez jelentős módszertani és széles körű vizsgálati feladatokat jelentett. A vörösvérsejtek membránjának megfelelő átjárhatóvá tétele (permeabilizálása) és a fehérjék rögzítése (fixálása) után, specifikus antitestek segítségével áramlási citométerben végezzük a mennyiségi meghatározásokat. Nagy feladat a megfelelő antitestek kiválasztása, titrálása, validálása, a genetikai tesztek beállítása, értékelése. Igen sokat segített, hogy száznál több munkatársunkat is sikerült meggyőzni arról, hogy egy ujjbegytűszúrást eltűrve vérmintát adjon a kontrollvizsgálatokhoz. Először a már ismertebb vörösvérsejt membránfehérjék mennyiségi analízisét végeztük el, és folyamatosan bővítve a palettát haladunk a kisebb mennyiségben jelen lévő, de a betegségek tekintetében akár fontosabb membránfehérjék vizsgálatához. A vörösvérsejt membránfehérjék új, megbízható adatbázisát Hegedűs Tamás és munkatársai fejlesztették ki, a molekuláris genetikai vizsgálatokban Orbán Tamás és munkatársai segítenek.
A vizsgálatainkkal megcélzott fő betegségcsoportok a sejtanyagcsere zavaraihoz kapcsolódnak, tehát az Alzheimer-kór, a köszvény és a cukorbetegség kerültek a középpontba. Jelenleg minden vércseppből párhuzamosan 15-20 membránfehérje, így a fő cukor-, koleszterin-, húgysav-, kalcium- és drogtranszporterek, valamint az inzulinreceptor szintjét mérjük, és a megfigyelt változások genetikai hátterét vizsgáljuk. Az eredmények jelentős nemzetközi folyóiratokban jelennek meg, és egyre szélesebb érdeklődést keltenek, míg a szabadalom gyakorlati hasznosítása főként a komplex betegségek diagnosztikája terén indulhat el. A szerteágazó laboratóriumi munkákban jelenleg főként Zámbó Boglárka, Mózner Orsolya és Kulin Anna vesz részt, a koordinációt Cserepes Judit végzi, míg a fehérjék szabályozását, sejten belüli mozgását Enyedi Ágnes, Homolya László és Bartos Zsuzsa vizsgálja. Kiváló klinikus partnereink az Alzheimer-vizsgálatokban Janka Zoltán és Fehér Ágnes, a köszvényes betegek esetében Poór Gyula és Pálinkás Márton, a cukorbetegek vizsgálatánál Korányi László, Schwab Richárd és Somogyi Anikó. A munkát több NKFI/OTKA (K115375, K127961, K128011, K128123, K119223) egy VEKOP (2.1.1-15-2016-00117) egy FIKP-EMMI és egy FIEK (16-1-2016-0005) pályázat is támogatja.•
Fontosabb hivatkozások
Sarkadi B, Várady Gy; Kasza I.: Quantitative determination of biomarkers in the erythrocyte cell membrane EP 2839293 B1, Patent appl., 2012.
Kasza I, Várady G, Andrikovics H, Koszarska M, Tordai A, Scheffer GL, Németh A, Szakács G, Sarkadi B.: Expression levels of the ABCG2 multidrug transporter in human erythrocytes correspond to pharmacologically relevant genetic variations. PLoS One. 2012, PMID: 23166586.
Várady G, Szabó E, Fehér Á, Németh A, Zámbó B, Pákáski M, Janka Z, Sarkadi B.: Alterations of membrane protein expression in red blood cells of Alzheimer’s disease patients. Alzheimers Dement (Amst). 2015, PMID: 27239515.
Zámbó B, Várady G, Padányi R, Szabó E, Németh A, Langó T, Enyedi Á, Sarkadi B.: Decreased calcium pump expression in human erythrocytes is connected to a minor haplotype in the ATP2B4 gene. Cell Calcium. 2017, PMID: 28216081.
Zámbó B, Bartos Z, Mózner O, Szabó E, Várady G, Poór G, Pálinkás M, Andrikovics H, Hegedűs T, Homolya L, Sarkadi B.: Clinically relevant mutations in the ABCG2 transporter uncovered by genetic analysis linked to erythrocyte membrane protein expression. Sci Rep. 2018, PMID: 29749379.